熔點與凝固點(Melting and Freezing Points )
熔點與凝固點(Melting and Freezing Points )
國立彰化高級中學賴文哲教師/國立彰化師範大學物理系洪連輝教授責任編輯
結晶的固體當溫度漸漸升高,直到發生熔化時的溫度稱為熔點,熔化時所增加的熱量用來破壞分子間的作用力(即改變位能),而分子動能並不增加,此時溫度維持固定。若反過來對液體降溫,直到其凝固時的溫度稱為凝固點。
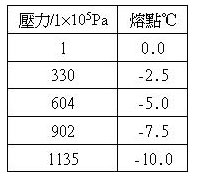
熔點的高低會受到壓力影響,其變化分為兩類:一類是當壓力升高則熔點降低,例如純水在一大氣壓時的熔點非常接近 $$0^\circ C$$,直接對低於 $$0^\circ C$$ 的冰塊加壓,則會使冰塊受壓而熔化,但這種因壓力變化而造成的熔點變化非常小,大約每升高 $$130$$ 個大氣壓降低 $$1$$ 攝氏度;另一類是當壓力升高則熔點升高,大部分物質具有此種特性。對於穿冰刀溜冰時摩擦力很小的原因,早期認為是因為冰刀接觸面積小,對冰的表面壓力大,造成冰面暫時的熔化,目前已了解是具有其他的表面作用。
一般非晶材料以及一些聚合物沒有一個真正的熔點,因為並非在特定的溫度突然相變,而是在熔化時溫度仍然漸進的改變,例如玻璃。正因為完全凝固的玻璃仍然沒有固定的結晶排列,有些數百年教堂的大玻璃,上方明顯比下面的部份來得厚。
還有些物質具有不同的固液轉變溫度,舉例來說,瓊脂(agar)在 $$85^\circ C$$ 融化並且在 $$31^\circ C$$ 至 $$40^\circ C$$ 之間凝固。元素中具有最高的熔點是鎢,為 $$3422^\circ C$$,用來作燈泡中燈絲的材料。熔點最低的是氦,在 $$-271.7^\circ C$$ 時就可熔化。
參考資料:
1. Melting point. http://en.wikipedia.org/wiki/Melting_point
2. Ice. http://en.wikipedia.org/wiki/Ice


 前一篇文章
前一篇文章 下一篇文章
下一篇文章
